発現変動遺伝子を確認後、上流解析を行うためには、代謝経路やシグナル伝達系など、一般的なパスウェイ(カノニカルパスウェイ)以外に、タンパク間相互作用 (PPI) や、遺伝子発現制御(転写制御)、共発現、文献情報などが必要となります(前回までの記事を参照)。
それらの上流解析に利用できる情報は、無料で入手しやすいものから、そうでないものもあります。もし、敷居が高いと感じられるのであれば、簡易的に上流解析を行うことを考えてはいかがでしょうか。
発現変動遺伝子を確認後、上流解析を行うためには、代謝経路やシグナル伝達系など、一般的なパスウェイ(カノニカルパスウェイ)以外に、タンパク間相互作用 (PPI) や、遺伝子発現制御(転写制御)、共発現、文献情報などが必要となります(前回までの記事を参照)。
それらの上流解析に利用できる情報は、無料で入手しやすいものから、そうでないものもあります。もし、敷居が高いと感じられるのであれば、簡易的に上流解析を行うことを考えてはいかがでしょうか。
GO解析とパスウェイ解析も、解析の原理は同じと以前述べました。どちらの解析方法を使っても、発現変動した遺伝子が、どの機能(パスウェイ)に多く含まれているのか、確認できます。
しかし、この両者には、発現変動した遺伝子どうしの関係が含まれているかどうかという違いがあります。アノテーションのGene Ontology (GO) には、相互作用の情報は存在しません。GOは、アポトーシス促進、抑制といった機能を表す言葉を持ちますが、どの遺伝子がどの遺伝子に対してという from, to の情報を持っていません。(これは、ヒートマップやGSEAにも言えることです。)
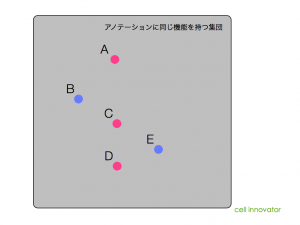
一方、パスウェイ(またはネットワーク)には、それらの相互作用の情報が含まれています。結合するのか、活性化するのか、抑制するのか、図に含まれる矢印から前後の関係を把握できます。
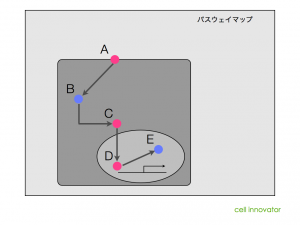
前回記事の補足として、マイクロアレイ解析の結果について、論文で記述する際の注意点を解説します。
「マイクロアレイ解析の結果、」に続く文章として、適切なものはどれでしょうか?
まず、 A はよくありません。レビューワーにスペキュレーションと見なされるかもしれません。理由は前回記事にあります。おそらく、「マイクロアレイ以外の他の実験結果を示せ」という注文がつくでしょう。
次に、B もよくありません。間違いではないかもしれませんが、「もう少し詳しく」と指摘されそうです。「脂質代謝系の遺伝子が活性化された可能性がある」ならよいでしょう。
C は問題ありません。無難な表現です。厳密には、脂質代謝系の遺伝子すべてが増加したわけではないでしょうから、後述の D がより無難な表現です。
D は事実のみを伝えているので、全く問題ありません。この事実をどう判断したのかは、著者の意見と明記して、追記しておけばよいでしょう。
マイクロアレイ解析のフローチャート2までに得られたのは、「特定の(生物学的な)機能を持ち、かつ、特定の発現変動パターンを示した遺伝子群」でした。例えば、「炎症系の遺伝子が増加していた」ということが分かったとしましょう。
次のステップに移る前に、まず、ここで考慮すべきポイントがあります。それは、「炎症系の遺伝子が増加していた」=「炎症反応が亢進した」ではない、ということです。
意外に思われる方も少なくないのではないでしょうか?ここにアノテーションの問題があります。
第1に、「炎症系の遺伝子」というアノテーションには、「炎症を活性化する遺伝子」と「炎症を抑制する遺伝子」の両方が含まれています。
GO:0006954: inflammatory response には、 GO:0050728: negative regulation of inflammatory response と GO:0050729: positive regulation of inflammatory response が含まれます。

第2に、アノテーションの情報は更新され続けており、完全ではありません。まだ、活性とも抑制とも書かれていないこともありますし、活性と抑制のどちらも書かれていることもあります。(おそらくは、ある条件下で逆の働きをすることもあるのでしょう。)例えば、 Angiotensinogen (AGT) は、 negative regulation of neuron apoptotic process と positive regulation of apoptotic process の両方をアノテーションに持ちます。
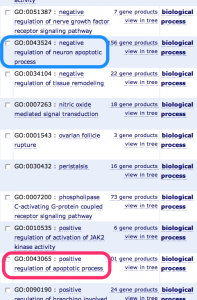
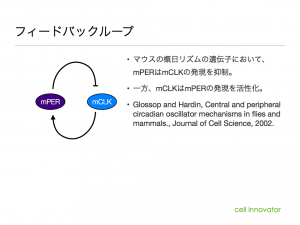
第3に生体内の多くの現象が、フィードバックにより恒常性を保っています。よって、ある現象を活性化させる遺伝子の発現が増加したとき、負のフィードバックが働き、その遺伝子を抑制する遺伝子も増加してくることが予想されます。したがって、ある現象を活性化する遺伝子と抑制する遺伝子の両方が増加していても、それほど不自然ではないと言えるでしょう。フィードバックループの例としては時計遺伝子がよく知られています。
例えば、肝硬変でコラーゲンの産生が過多になっているような組織であれば、コラーゲンの遺伝子である COL1A1 の発現が高く、同時にコラーゲンを分解する MMP の発現も高いという状況が予想されます。MMPによる分解が追いついていないだけと考えれば、矛盾した状態とは言えないでしょう。
以上のようなことから、マイクロアレイデータのみを根拠に、「炎症系の遺伝子が増加していた」=「炎症反応が亢進した」と結論づけることは困難と考えられます。
発現変動遺伝子の抽出後、まず、必要なことは、増加、減少した遺伝子(発現変動遺伝子)が、どのような遺伝子であるかを分析することです。この方法は、大きく分けて、次の2通りの方法のいずれかを用います。
A. (生物学的な)機能で見る。
B. 発現変動のパターンで見る。
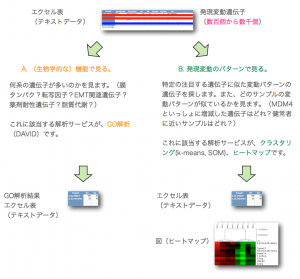
何系の遺伝子が多いのかを見ます。(膜タンパク?転写因子?EMT関連遺伝子?薬剤耐性遺伝子?脂質代謝?) これに該当する解析が、GO解析(DAVIDなどを使用)です。
特定の注目する遺伝子に似た変動パターンの遺伝子を探します。また、どのサンプルの変動パターンが似ているかを見ます。(MDM4といっしょに増減した遺伝子はどれ?健常者に近いサンプルはどれ?) これに該当する解析が、クラスタリング(k-means, SOM)、ヒートマップです。
このA., B. の2通りの解析は、独立したものではなく、また、それだけでは終わりません。GO解析の結果をさらにヒートマップで表示して、発現変動変動のパターンを確認するケース(A. –> B.)や、特定の発現変動パターンの遺伝子を選択して、その機能をGO解析で確認するケース(B. –> A.) が通常です。それぞれの解析を単独で行っても効果的ではありません。(セルイノベーターの解析サービスでは、初めからこれらの解析サービスを含めて提供しています。)
解析はさらに続きます。
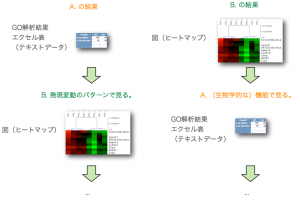
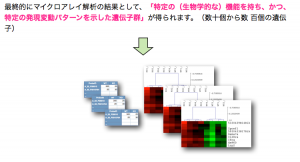
最終的にマイクロアレイ解析の結果として、「特定の(生物学的な)機能を持ち、かつ、特定の発現変動パターンを示した遺伝子群」が得られます。(数十個から数 百個の遺伝子)